Como realizar diluições em série
Autor:
Roger Morrison
Data De Criação:
19 Setembro 2021
Data De Atualização:
11 Poderia 2024
Contente
- estágios
- Método 1 Realize uma diluição simples
- Método 2 de 2: Calcular o fator de diluição final e a concentração
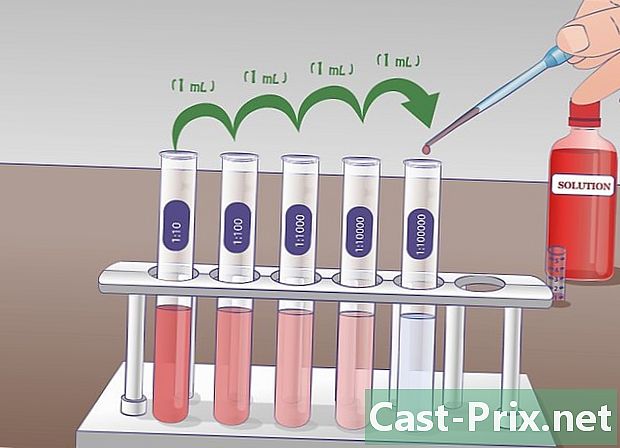
Na química, uma diluição consiste em reduzir a concentração de uma determinada solução. Uma diluição em série é simplesmente uma diluição repetida de uma solução original para amplificar rapidamente o fator de diluição. Esse tipo de diluição é frequentemente realizado durante experimentos que exigem soluções altamente diluídas e alta precisão, como aquelas envolvendo curvas de concentração em escala logarítmica ou aquelas que permitem o cálculo da densidade de bactérias em determinados meios. Eles são frequentemente realizados em bioquímica, microbiologia, farmacologia ou química.
estágios
Método 1 Realize uma diluição simples
-

Determine o líquido diluente certo (ou diluente). A escolha do diluente é muito importante e depende da solução que você deseja diluir. O diluente é frequentemente água destilada, mas não é sistemático. Assim, com uma solução contendo bactérias ou células, um meio de cultura é usado. Para diluição em série, o mesmo diluente é usado em todos os tubos.- Se você não souber qual diluente usar, obtenha ajuda de uma pessoa competente ou procure na Internet o que as pessoas precisam fazer para obter uma experiência semelhante.
-
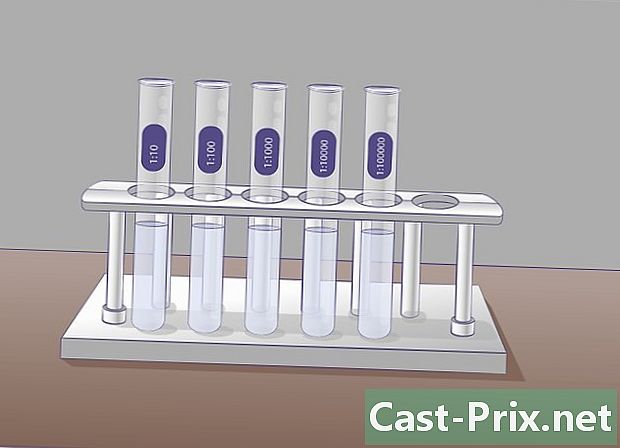
Prepare vários tubos de ensaio contendo 9 ml de um líquido de diluição. Estes tubos de ensaio serão utilizados para fazer diluições sucessivas. O princípio é simples: você irá colher uma amostra da solução inicial e transferi-la para o próximo tubo. Depois, colherá uma amostra deste tubo para colocá-lo no próximo, etc.- Antes de iniciar as diluições, é aconselhável identificar antecipadamente os tubos de ensaio para evitar confusão posteriormente.
- Em cada tubo, você terá uma concentração dez menor que a anterior. O primeiro tubo conterá uma solução diluída no décimo, segundo, centésimo, terceiro, milésimo e assim por diante. Determine com antecedência o número de diluições para evitar a fabricação de mais tubos do que o necessário e desperdice o diluente desnecessariamente.
-
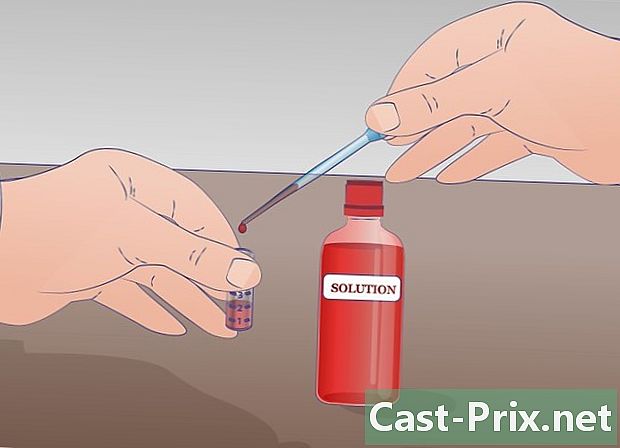
Prepare um tubo de ensaio com a solução da sua mãe. Coloque pelo menos 2 ml. A quantidade mínima de solução-mãe para diluição em série é de um mililitro. Permita 2 ml para uma possível segunda diluição. Este tubo de solução mãe, você pode marcar um "SM".- Antes de iniciar uma diluição em série, misture bem a solução inicial.
-
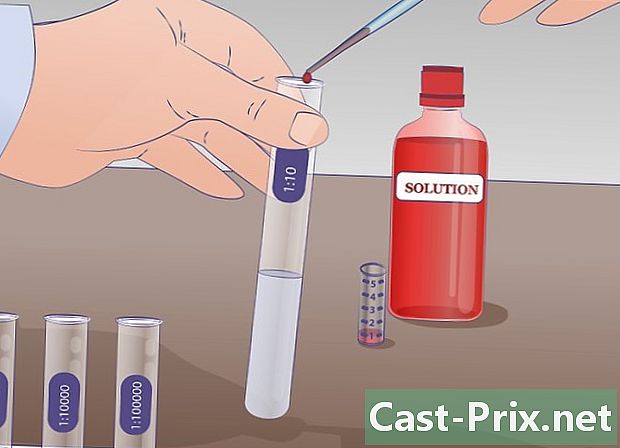
Faça a primeira diluição. Pipete 1 ml da solução-mãe para o tubo de ensaio rotulado "SM" e transfira essa quantidade para o tubo de ensaio rotulado. 1/10 que já contém 9 ml de líquido de diluição. Misture para obter uma solução homogênea. Neste tubo, agora existem 10 ml de solução: 1 ml de solução-mãe e 9 ml de líquido de diluição. Esta nova solução é dez vezes menos concentrada que a anterior. -
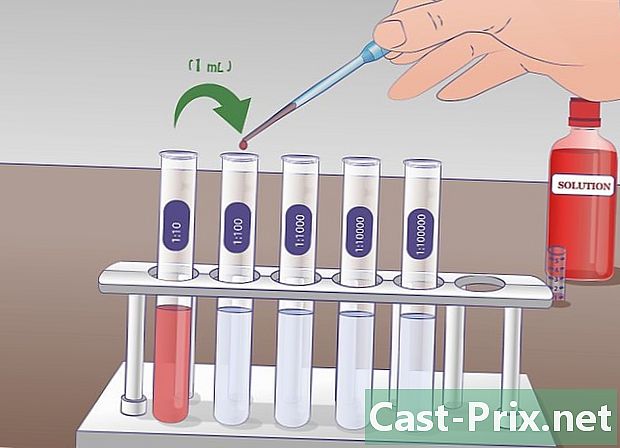
Realize a segunda diluição. Na segunda diluição em série, você extrairá 1 ml da solução do tubo rotulado 1/10 e você vai derramar no tubo 1/100 que já contém 9 ml de líquido de diluição. O tubo 1/10 terá sido bem misturado antes da amostragem. Depois que a transferência estiver concluída, misture bem o tubo 1/100. A solução do tubo marcado 1/10 é 10 vezes mais concentrado que o do tubo rotulado 1/100. -

Repita essa manipulação, se necessário. Este procedimento pode ser repetido quantas vezes desejar até que a diluição desejada seja alcançada. Para um experimento envolvendo curvas de concentração, é possível obter uma série de soluções com diluições para a unidade, a décima (1/10), a centésima (1/100) ou a milésima (1/1000).
Método 2 de 2: Calcular o fator de diluição final e a concentração
-

Calcular o proporção a diluição final após diluição em série. A razão total de diluição é obtida multiplicando o fator de diluição por si só quantas vezes houver diluições. Matematicamente, a fórmula é a seguinte: Dt = D1 x D2 x D3 x ... x Dncom Dt representando o fator de diluição total e Dn, a razão da diluição.- Então, vamos supor que você faça uma diluição de 1/10 de um líquido 4 vezes seguidas. Na fórmula, substitua o fator de diluição pelo seu valor: Dt = 10 x 10 x 10 x 10 = 10.000
- O fator de diluição final do quarto tubo na sua diluição em série é de 1/10.000. A concentração da solução do último tubo agora é 10.000 vezes menor que a da solução original.
-

Determine a concentração de uma solução após a diluição. Para encontrar a concentração final de uma solução após diluição em série, é necessário conhecer a concentração inicial. A fórmula é então: Cfinal = Cinicial/ Acom Cfinal representando a concentração terminal da solução diluída, Cinicial, a concentração da solução-mãe e D, a razão da diluição previamente determinada.- Portanto, se você diluir uma solução celular com uma concentração de 1.000.000 células por ml e sua taxa de diluição for definida como 1.000, qual será a concentração final da sua amostra diluída?
- Use a fórmula:
- Cfinal = Cinicial/ A
- Cfinal = 1 000 000/1 000
- Cfinal = 1000 células / ml
-

Preste atenção às unidades usadas. Ao fazer seus cálculos, verifique sempre se você está usando as mesmas unidades. Assim, se você começar a partir de uma concentração de células por ml, seu resultado final também será em células por ml. Se a sua concentração inicial for em partes por milhão (ppm), sua concentração final será em partes por milhão.

